Ce processus est couplé à la respiration cellulaire, implique O2 et est beaucoup plus efficace que l’oxydation anaérobie. Au lieu de 2 ATP, l’oxydation aérobie génère 38 ATP par le glucose. Il peut également oxyder les acides gras et les parties carbonatées des acides aminés.
Le cycle de Krebs: cycle de l’acide citrique
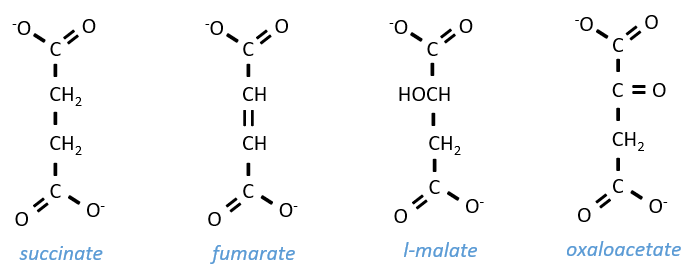
Szent Fuorgue a étudié la respiration cellulaire à partir d’un extrait de muscle. Il a analysé l’absorption d’O2 en présence de diverses molécules. Il a observé que certains d’entre eux augmentent considérablement l’absorption d’oxygène par les tissus. C’est le cas pour le succinate et le fumarate.
Ces molécules sont stables aux variations de la température. La combustion d’un succinate consomme normalement 3 O2 mais pendant les expériences, ils ont observé que l’absorption d’oxygène était au-dessus de cette valeur. Ils ont également montré que l’absorption peut être diminuée si l’on ajoute du malate au système. Le malate est un inhibiteur qui affecte l’oxaloacétate, un catalyseur du cycle de Krebs qui est régénéré à chaque cycle sauf en présence de malate.
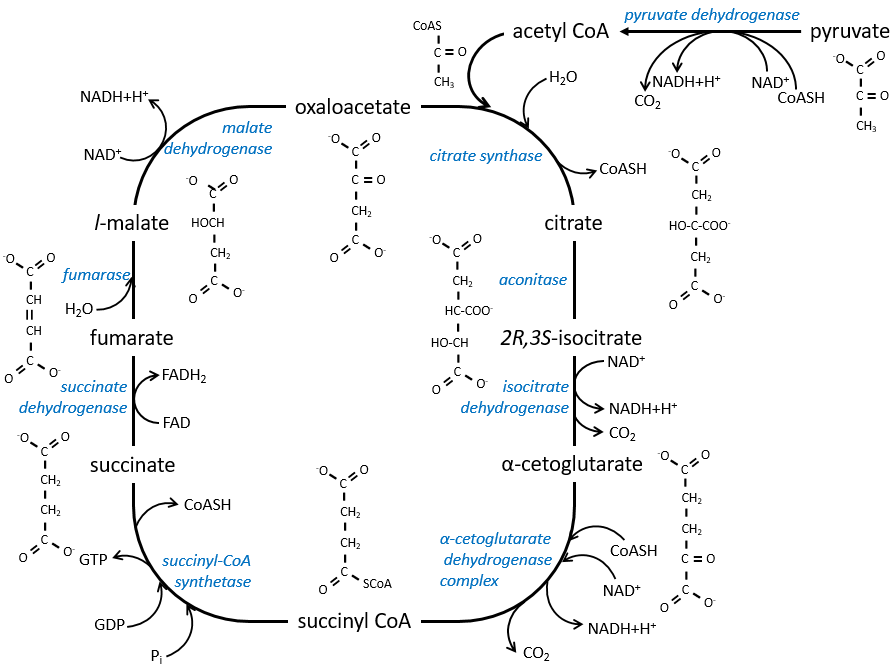
Le cycle peut être repris par la figure suivante :
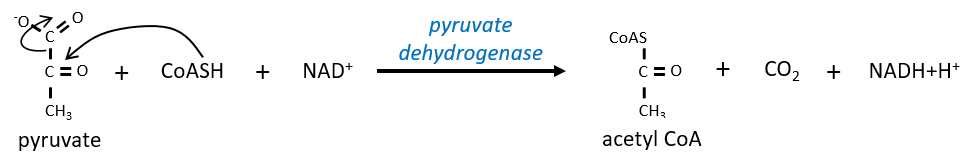
Le citrate est le produit de la première réaction du cycle. Avant d’expliquer le cycle, nous allons expliquer la formation de l’acétyl CoA. Il est fabriqué à partir de pyruvate. La première étape est la substitution d’un CO2 par le COASH par une liaison thioester.
La réaction est irréversible (libération de CO2) et est catalysée par une grande enzyme: la pyruvate déshydrogénase. À l’intérieur de l’enzyme, on trouve la vitamine B1. Simultanément, il y a une oxydation faite par le NAD +. Le produit est l’acétyl coenzyme A, ou l’acétyl-coA.
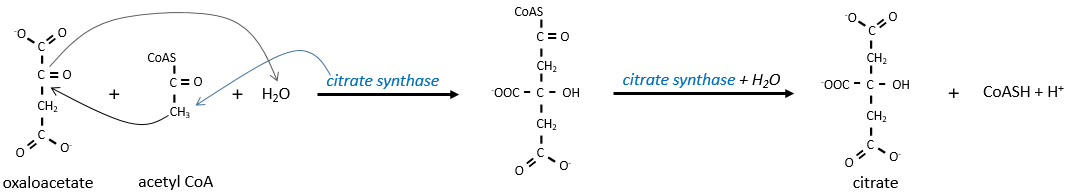
La première étape forme le citrate par la condensation entre l’acétyl-coA et l’oxaloacétate. La réaction est aidée par la citrate synthétase qui prend un proton du groupe méthyle de l’acétylCoA. Il libère la coenzyme qui peut être utilisée à nouveau.
Le citrate est symétrique mais il est considéré comme prochiral par l’enzyme de la réaction suivante. Pour poursuivre le cycle, l’aconitase change la conformation du citrate pour obtenir l’isocitrate.
L’équilibre est fortement en faveur de la gauche mais l’espèce droite est consommée par les réactions suivantes de sorte que la réaction est déplacée vers la droite. L’étape 3 est subdivisée en une réaction d’oxydation et une décarboxylation.
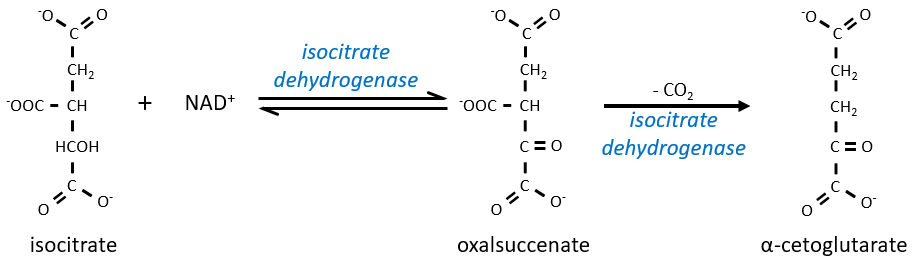
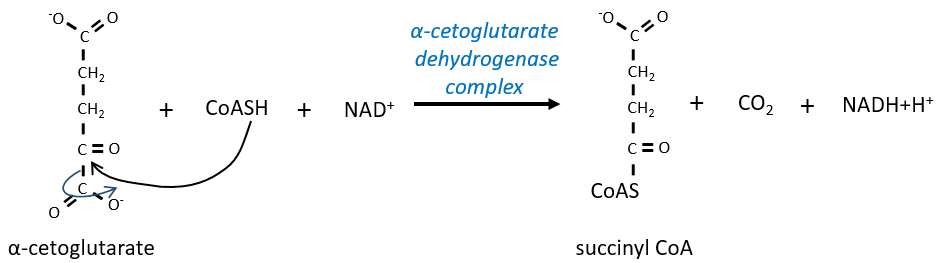
L’étape 4 est similaire à la formation de l’acétyl-CoA et conduit à la formation du succinyl-coA.
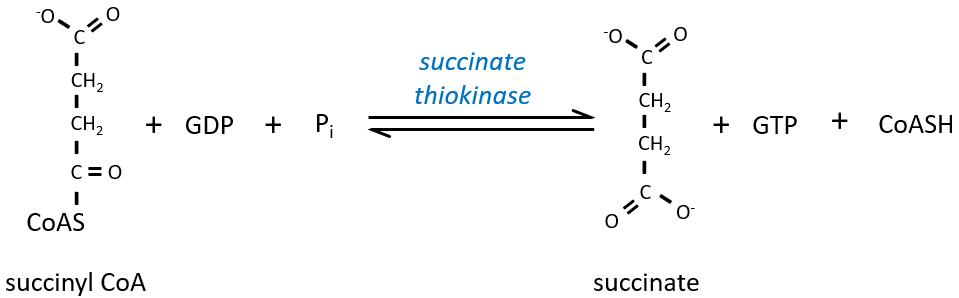
Le clivage de la liaison thioester fournit suffisamment d’énergie pour former, non pas un ATP mais un GTP.
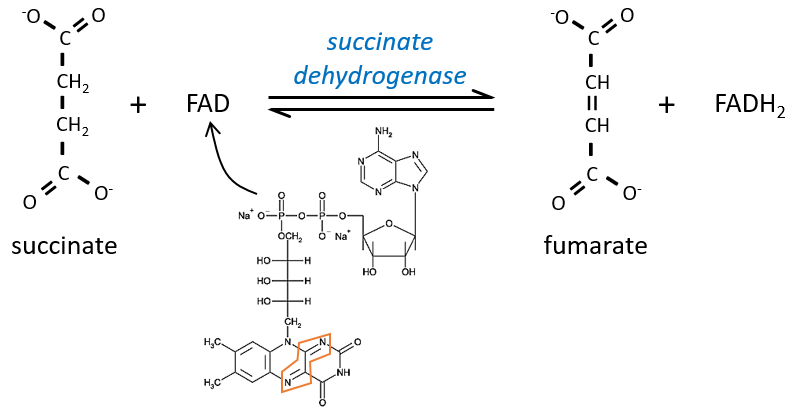
Le succinate est ensuite oxydé pour le fumarate. Le cofacteur est le FAD: Flavin adénine dinucléotide, un dérivé de la riboflavine (vitamine B2).
La réduction du FAD se fait dans la zone orange.
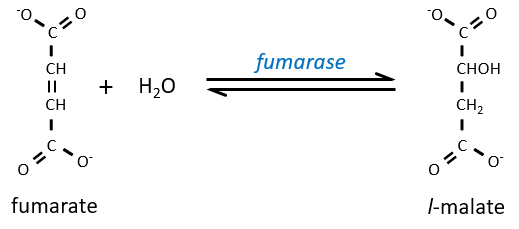
L’étape 7 nécessite une molécule d’eau pour former le malate. Le malate est une molécule chirale, la chiralité donnée par la structure du site actif de l’enzyme. En conséquence, seul le l-malate est obtenu.
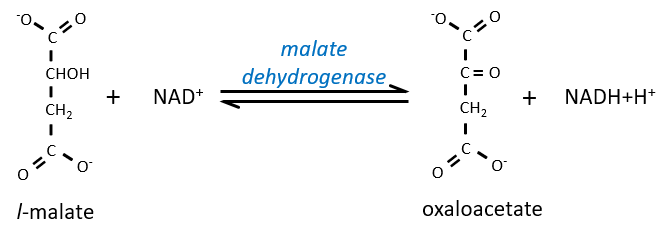
Enfin, l’oxaloacétate est régénéré à partir du malate.
Maintenant, vous pouvez dire qu’il n’y a aucun des 38 ATP promis au début de la section. Un seul GTP a été formé pendant le cycle mais plusieurs CO2 ont été rejetés et 3 NAD + et un FAD ont été réduits. Ces molécules représentent l’énergie de l’ATP. En outre, c’est le processus qui se produit dans les cellules aérobies, mais aucun O2 n’a jamais été impliqué dans le cycle. Nous verrons la source de l’ATP dans la section suivante: la chaîne respiratoire.